Le plan d’analyse statistique (PAS) est un document fondamental en recherche clinique et dans la conduite des essais cliniques. Il décrit de manière prospective la stratégie d’analyse des données afin de garantir la validité scientifique, la transparence et la reproductibilité des résultats.
Conformément aux lignes directrices ICH E9, le PAS constitue un document distinct du protocole d’étude. Il formalise les principes statistiques appliqués aux critères d’évaluation, aux populations d’analyse et à l’interprétation des résultats, dans un cadre réglementaire strict.
Les évolutions récentes des recommandations, notamment ICH E9(R1), ont renforcé le rôle du PAS à travers l’introduction de la notion d’estimand, visant à aligner explicitement la question clinique, le design de l’étude et la méthode d’analyse statistique.
Dans cet article, nous présentons le rôle, l’utilité et la justification réglementaire du plan d’analyse statistique (PAS) en recherche clinique.
Nous abordons également les éléments essentiels et recommandés pour son élaboration, conformément aux lignes directrices ICH E9 et à la notion d’estimand.
L’article aborde notamment :
- le rôle et l’utilité du plan d’analyse statistique en recherche clinique ;
- le cadre réglementaire du PAS et les recommandations ICH E9 ;
- la place de la notion d’estimand dans la stratégie d’analyse ;
- les éléments méthodologiques à considérer lors de l’élaboration d’un plan d’analyse statistique.

Rôle, utilité et justification réglementaire du Plan d’analyse statistique
Un plan d’analyse statistique, souvent abrégé en PAS, est un document technique rédigé par le statisticien pour compléter le protocole d’une étude clinique. Il décrit de façon détaillée la manière dont les données seront analysées, mais aussi la façon dont les résultats seront présentés dans le rapport statistico-clinique, à travers les tableaux, graphiques et analyses attendus. Le PAS anticipe ainsi le rapport statistique final de l’étude.
Le PAS doit être rédigé bien avant la fin des inclusions des participants. Son objectif est de définir et figer la méthodologie d’analyse avant la fin de l’étude afin d’éviter toute adaptation des analyses aux données observées. Cette anticipation est essentielle pour limiter les analyses a posteriori orientées par les résultats et garantir la cohérence entre les objectifs initiaux et les analyses réalisées.
Au-delà de la description des méthodes statistiques, le PAS développe les aspects cliniques susceptibles d’avoir un impact sur les données et leur analyse. Il transforme les objectifs scientifiques de l’étude en hypothèses statistiques analysables, traduit les critères principaux et secondaires en variables mesurables, et définit les populations d’analyse, les déviations au protocole, la taille de l’échantillon ainsi que les analyses intermédiaires planifiées.
D’un point de vue réglementaire, le PAS répond aux exigences des lignes directrices ICH E9, qui recommandent la rédaction d’un document distinct du protocole détaillant l’ensemble des méthodes statistiques prévues. Cette séparation entre planification et exécution de l’analyse constitue un élément clé pour les autorités réglementaires, car elle renforce la transparence, la reproductibilité et la crédibilité des résultats d’un essai clinique.
Cadre réglementaire du Plan d’Analyse Statistique et notion d’estimand
Le Plan d’Analyse Statistique s’inscrit dans un cadre réglementaire strict, défini notamment par les lignes directrices ICH E9 relatives aux principes statistiques des essais cliniques. Ces recommandations imposent que la stratégie d’analyse soit définie de manière prospective, documentée et cohérente avec les objectifs scientifiques de l’étude.
La révision ICH E9(R1) a introduit la notion d’estimand, qui constitue aujourd’hui un élément central du PAS.
Un estimand décrit précisément ce qui doit être estimé pour répondre à une question clinique donnée, en tenant compte de la population ciblée, de la variable d’intérêt, des événements intercurrents (arrêt de traitement, changement de traitement, données manquantes, etc.) et de la méthode de résumé statistique.
L’introduction des estimands vise ainsi à aligner de manière explicite la question clinique, le design de l’étude, la gestion des événements intercurrents et la méthode d’analyse statistique.
Dans ce contexte, le PAS joue un rôle clé en assurant la traduction opérationnelle des estimands définis dans le protocole. Il précise comment les données seront analysées pour estimer l’effet du traitement conformément à la question clinique posée, et comment les événements interférants seront pris en compte dans l’analyse. Cette approche renforce la cohérence entre les objectifs cliniques, les hypothèses statistiques et les méthodes d’analyse, tout en limitant les ambiguïtés d’interprétation des résultats.
Comment élaborer un plan d’Analyse Statistique ?
Rédiger un Plan d’analyse statistique nécessite de solides compétences statistiques et cliniques. Généralement réalisé par un statisticien en collaboration avec l’équipe clinique, le PAS doit cerner tous les points scientifiques pour une meilleure gestion et réduction des biais. Il en est de même pour une meilleure communication des résultats dans le rapport statistique de l’essai clinique.
Que contient un plan d’analyse statistique ?

Bien que les lignes directrices ICH E9 et SPIRIT exigent l’existence d’un plan d’analyse statistique distinct du protocole, elles ne définissent pas une structure unique ou figée. En pratique, plusieurs recommandations internationales proposent toutefois un contenu minimal standardisé, permettant d’assurer la transparence des analyses, leur traçabilité et leur conformité réglementaire.
Le PAS a pour objectif de documenter de manière anticipée l’ensemble des choix méthodologiques et statistiques de l’étude, avant l’accès aux données finales. Il explique comment et pourquoi certains points sont développés, afin de garantir une analyse cohérente avec les objectifs scientifiques et cliniques de l’essai.
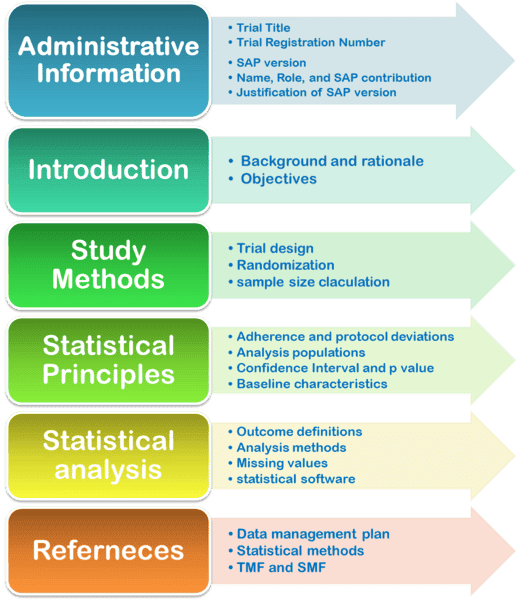
1. Informations administratives de l’étude
Le PAS reprend la partie administrative de l’étude essentielle à son identification réglementaire. Elle permet de rattacher le document au protocole de l’étude et d’en assurer le suivi tout au long du cycle de vie du projet.
Cette section inclut généralement :
- le numéro et le titre du protocole,
- la version du protocole et du PAS,
- la date de validation du document,
- les rôles et responsabilités des acteurs de l’étude (sponsor, statisticien, CRO, le cas échéant),
- les références réglementaires applicables.
2. Introduction, objectifs et design de l’étude
Le PAS est distinct du protocole, il doit donc reprendre et de façon synthétique tous les éléments clés nécessaires à la compréhension du cadre scientifique de l’étude.
On y retrouve notamment :
- le design de l’étude (randomisée, contrôlée, en ouvert, en double aveugle, etc.),
- les objectifs principaux et secondaires,
- la définition précise des critères de jugement,
- le cadre des tests d’hypothèse (supériorité, non-infériorité ou équivalence).
Cette partie assure la cohérence entre les objectifs cliniques et les analyses statistiques prévues.

3. Aspects méthodologiques ayant un impact statistique
Le PAS doit détailler l’ensemble des éléments méthodologiques susceptibles d’influencer l’analyse des données et l’interprétation des résultats.
Il précise notamment :
- La procédure de randomisation et les modalités.
- Les analyses intermédiaires prévues et leurs justifications. Il est également recommandé de préciser les dates prévues pour leur réalisation. Il en est de même pour les dates de disposition des données et le début de l’analyse statistique finale.
- La définition des populations d’analyse (ITT, PP, Safety, etc.), en précisant explicitement quelle population est utilisée pour l’analyse de chaque critère de jugement, afin d’éviter toute ambiguïté dans l’interprétation des résultats. Cette distinction est essentielle, car l’analyse d’un critère principal en intention de traiter (ITT) peut conduire à des conclusions différentes de celles obtenues en per protocole (PP). Le PAS doit donc expliciter clairement le lien entre chaque critère et la population d’analyse retenue.
(voir aussi : population ITT vs PP) - Les déviations au protocole pertinentes pour l’analyse,
- Les caractéristiques démographiques et cliniques de base des participants.
Ces éléments sont indispensables pour anticiper les biais potentiels et assurer la robustesse des analyses.
4. Gestion des données et taille d’échantillon
Les données étant au cœur de toute analyse statistique, le PAS décrit les principes généraux de leur gestion, sans se substituer au Plan de Data Management.
Cette section précise :
- La justification et le calcul de la taille d’échantillon et les hypothèses retenues,
- l’état de la base de données au moment de l’analyse statistique,
- les règles de gel de base,
- les méthodes de gestion des données manquantes (par exemple : imputation multiple, analyses de sensibilité).
Le PAS fait ainsi le lien entre la stratégie de collecte des données et leur exploitation statistique.
5. Méthodologie d’analyse statistique
Cette partie est le cœur du plan d’analyse statistique. Elle doit décrire de façon détaillée toutes les analyses prévues, afin qu’elles puissent être reproduites sans ambiguïté.
Elle comprend notamment :
- les statistiques descriptives utilisées pour chaque variables quantitatives et qualitatives,
- les méthodes d’analyse des critères principaux et secondaires,
Cette partie doit définir les variables d’intérêt pour chaque critère d’évaluation ainsi que les méthodes de leurs descriptions, de comparaison ou corrélation. - les tests statistiques paramétriques et non paramétriques à appliquer,
- les vérifications des hypothèses statistiques (normalité, homogénéité, etc.),
- les modèles statistiques utilisés, le cas échéant,
- les méthodes et tests de sensibilité,
- les analyses en sous-groupes ou ajustées sur covariables,
- les règles de calcul et transformation des variables dérivées
(baseline, variations, temps jusqu’à événement, etc.).
6. Seuil de significativité et logiciels statistiques
Le PAS précise également le cadre d’interprétation des résultats statistiques.
On y retrouve :
- le risque d’erreur alpha retenu ou degrés de significativité des tests,
- les ajustements pour comparaisons multiples si nécessaires,
- le logiciel statistique utilisé (SAS, R, SPSS, etc.) ainsi que sa version.
7. Références et annexes
Enfin, le plan d’analyse statistique doit inclure les éléments permettant de justifier les choix méthodologiques et d’assurer la traçabilité documentaire.
Cette section comprend :
- les références méthodologiques et bibliographiques,
- les lignes directrices réglementaires,
- les annexes pertinentes (TLG, Plan de Data Management, TMF, SMF).

Conclusion
En résumé, le Plan d’Analyse Statistique est un document réglementaire essentiel au bon déroulement d’un essai clinique.
Son rôle est de définir de manière prospective, rigoureuse et transparente l’ensemble des analyses statistiques de l’étude, en cohérence avec les objectifs scientifiques et les exigences réglementaires.
Le PAS constitue ainsi une garantie de qualité méthodologique et de crédibilité scientifique vis-à-vis des autorités de santé. Toute modification apportée au Plan d’Analyse Statistique doit être strictement encadrée, justifiée et documentée, afin de préserver la validité des résultats, leur interprétation et la confiance portée aux conclusions de l’étude.